如果没有一些现代分析手段,那么当反应发生完全后,应尽快过滤,把沉淀分离出来洗净单独研究。对于强还原性的体系来说,空气中的氧也是一个不可忽略的因素。
关于硫代硫酸钠与硫酸铜反应的简单探究实验
实验目的:确定硫代硫酸钠与硫酸铜反应的化学方程式
那么,实验开始
实验环境温度:23℃
量取50ml水,加入2.5g五水合硫代硫酸钠,配成A液
量取50ml水,加入2.5g五水合硫酸铜,配成B液

3.取9个试管,往每个试管里都加入30滴B液
将试管编号为1~9
按序号,从小到大依次滴加A液
5,10,15,20,30,40,50,60,70滴

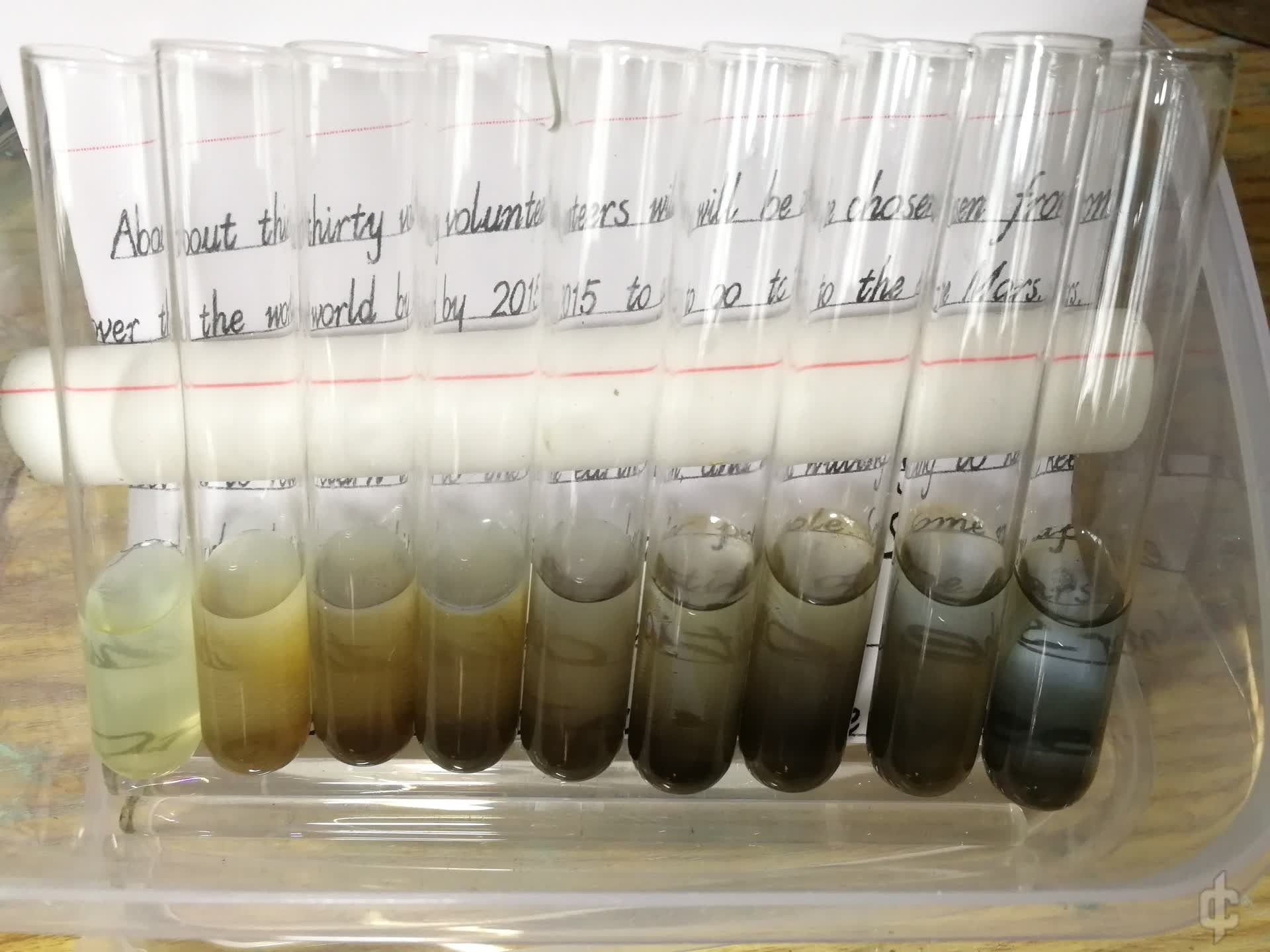
如图所示,按序号依次排列的试管(最右侧为1号,即为只滴加5滴硫代硫酸钠溶液的试管)
用“补纯净水”的方式,让各个试管液面基本平齐

静置约20min后,一些试管内溶液变得混浊

(为了方便表现混浊,在背后垫了印有文字的纸)
1号与2号试管基本保持澄清
3号与4号稍显混浊
5号较为澄清
6,7,8号又变得混浊
9号稍显混浊,但比7,8号澄清
实验结束
。。。
那么,实验结论呢
在不久之前,我与一些人讨论过这个反应,结论如下
硫代硫酸根将铜离子还原为亚铜离子,接着,亚铜离子与硫代硫酸根配位,这也是溶液产生绿色的原因
硫代硫酸根不稳定,会歧化生成硫单质,这是溶液变混浊(产生沉淀)的原因
另外,如果硫代硫酸钠大过量,最终会生成一种黑色的沉淀(在这个实验中没有出现,有可能是硫代硫酸钠未过量或反应时间不足所致),这是由反应S2O32-+S+Cu+=S4O62-+Cu2S导致的
(这个沉淀也不一定只是硫化亚铜,S与Cu的数量比在0.5~1之间,也就是说,如果硫代硫酸钠的量不同,可能会产生沉淀Cu1.8S,Cu1.5S...)
那么,结束了吗
在此之前,我个人做过与这个反应相关的一些很粗略的实验。并在混合两种物质的溶液时,得到了一种黄色的产物。

根据先前的推测,你可能会认为,这个沉淀就是单质硫
但是,沉淀放置几小时后...
如下图

最后
如下图,这是沉淀放置一周以上后的效果

这种黄色产物,似乎是Cu与S以某种比例形成的化合物
那么,我们最开始做的实验中,那个让溶液变混浊的沉淀是单质硫,还是类似于这个亮黄色固体的东西?
为什么硫与铜或亚铜的化合物会是亮黄色的?
...
硫代硫酸钠与硫酸铜的反应,似乎还有一些地方有些模糊不清
为了扫除这些模糊不清的地方,我写了这个帖子,希望有人能对于模糊不清的地方做出解释。
当然,这不是提问帖,如果没有人回答,我也会尽量想办法找出较为合理的答案。
我可能会继续做一些相关实验,然后发到这里
文章有许多不严谨之处,见谅
附上相关参考文献
黑黑的应该是氧化铜吧
遮盖了硫单质的颜色
变化的原因可能是漫长时间中 氢氧化铜失水和体系变碱性(二氧化硫溢出)
硫化铜可能性不高 因为硫化铜在空气中也会慢慢被氧化 变成氧化铜和硫
200字以内,仅用于支线交流,主线讨论请采用回复功能。
溶液静置约12h后
如图,似乎与之前结论说的“硫代硫酸钠大过量后出现黑色沉淀”不符
200字以内,仅用于支线交流,主线讨论请采用回复功能。
如图,放置约一个星期后

这是左边三个试管(7,8,9号)

200字以内,仅用于支线交流,主线讨论请采用回复功能。
进行“沉淀复现”
称量7.5g硫酸铜,配置成浓溶液

接着将溶液倒入量筒,用水将溶液补至90ml

这样就大致得到0.33mol/L的硫酸铜溶液
接着,如法配置同浓度的硫代硫酸钠溶液
选取三个培养皿,编号为1,2,3
1号 加入15ml之前配制的硫酸铜溶液与30ml硫代硫酸钠溶液,并加盖
2号 加入15ml硫酸铜溶液与30ml硫代硫酸钠溶液,不加盖
3号 加入15ml硫酸铜溶液与25ml硫代硫酸钠溶液,并加盖

这里从右往左依次为1,2,3
等待沉淀出现
200字以内,仅用于支线交流,主线讨论请采用回复功能。
取出编号3
如图,上层出现薄薄的一层翠绿色物质,底下则为黄色沉淀

顶部的绿色物质密度似乎比黄色沉淀要轻的多,用水直接清洗培养皿,倒去上层的水,便可将二者粗略分离

取出部分下层的黄色沉淀,分三份分别加入三支试管,编号1,2,3
1号加入30%H2SO4溶液2ml
2号加入30%H2SO4溶液2ml,然后加入一些KClO3固体
3号加水
如图,从左到右依次为编号1,2,3
反应约10min后

下图,为反应约20min后

(注:KClO3为KCl电解获得,可能存在KClO4与KCl杂质)
200字以内,仅用于支线交流,主线讨论请采用回复功能。
将黄色沉淀加入瓷舟中,编号为A
将硫代硫酸钠与草酸混合后制得的单质硫加入另一个瓷舟,编号为B
准备加热,图中下方装着亮黄色固体的瓷舟为A

如图



由此可初步推断
这个黄色沉淀不是硫单质,
而很有可能是硫与铜的化合物
200字以内,仅用于支线交流,主线讨论请采用回复功能。
补充
瓷舟加热实验中,单质硫是很久以前用硫代硫酸钠与草酸制备的
另外,为什么没有人讨论...
200字以内,仅用于支线交流,主线讨论请采用回复功能。
2Cu2++2S2O32-+2H2O===Cu2S+S+2SO42-+4H+
此反应常在分析化学中除去铜
200字以内,仅用于支线交流,主线讨论请采用回复功能。
将黄色沉淀加入瓷舟中,编号为A将硫代硫酸钠与草酸混合后制得的单质硫加入另一个瓷舟,编号为B准备加热,...
用盐酸溶解黑色产物
如果有硫化氢味道则含有硫化铜(估计这样加热曾经有硫化铜 也变成氧化铜了)
如果有蓝翠色溶液则含有氧化铜
单质硫如果曾经存在 这样加热后也早升华 加热前应该准备收集升华物以判断
200字以内,仅用于支线交流,主线讨论请采用回复功能。
2Cu2++2S2O32-+2H2O===Cu2S+S+2SO42-+4H+此反应常在分析化学中除去...
是我读书少了(╥ω╥`)
但是根据文献的说法,如果硫代硫酸钠不过量
应该会生成CuxS(1<x<2)?
虽然这个实验和文献中的实验有所区别...
200字以内,仅用于支线交流,主线讨论请采用回复功能。
200字以内,仅用于支线交流,主线讨论请采用回复功能。
用盐酸溶解黑色产物如果有硫化氢味道则含有硫化铜(估计这样加热曾经有硫化铜 也变成氧化铜了)如果有蓝翠...
30%硫酸和之前瓷舟中的黑色物质反应
这是加热前

这是加热后

溶液仍然显酸性,说明酸未反应完全,然而还有一部分黑色物质未溶解
200字以内,仅用于支线交流,主线讨论请采用回复功能。
30%硫酸和之前瓷舟中的黑色物质反应这是加热前这是加热后溶液仍然显酸性,说明酸未反应完全,然而还有一...
之后加入过量硝酸钾,似乎仍然有一小坨东西未溶解

然后加入氯酸钾

基本说明是硫铜化合物
200字以内,仅用于支线交流,主线讨论请采用回复功能。
然而,问题来了...
铜,银,金的硫化物全都是黑色或接近黑色的...[1]
虽然参考文献中的Cu2S为黄色,但毕竟那是个膜,而实验中做出来的却是厚厚的黄色固体沉淀
如果硫代硫酸钠与铜反应真的是Cu2S和S单质,那么最后的沉淀应该是黑色才对
如果反应产物是纯粹的单质S,那就更不可能了
除非
硫铜化物不一定是黑色
可能不是硫铜化合物
[1]《元素化学》格林伍德下册415页
另外,[北师大等]无机化学第四版706页
松田大佬应该是从这里找到硫代硫酸钠和硫酸铜的反应的式子吧...
然而按照这本书所写,反应现象应该是生成黑色或接近黑色沉淀,而不是黄色...




200字以内,仅用于支线交流,主线讨论请采用回复功能。