国内大部分有机化学教科书,在讲到苯分子结构时都会这样讲述:苯分子中6个C-C键是等同的,存在大π键(离域π键或者π电子离域)并不存在单双键交替的情况,凯库勒式实际上是错误的,只是由于历史的原因仍然沿用而已。某些教科书会用分子轨道(MO)理论进一步解释苯分子的π电子离域,6个π电子原子轨道彼此作用形成6个π分子轨道,6个π电子正好填满3个成键轨道,导致苯分子中6个C-C键完全等同,苯分子存在较大的离域能,因此苯环很稳定,容易发生取代反应而不是加成反应,也就是“芳香性”。
确实大部分教科书上都是这样介绍的,中学化学教科书更是强调“苯分子结构决不是单双键交替的环状结构”,教辅资料中的苯分子结构式,以及老师和同学们写苯结构式时,都习惯在正六边形中画一个圆圈表示,难道单双键交替的凯库勒式真的只是因为历史原因才沿用到今天的?
苯容易发生取代反应,不容易发生加成反应,证明了凯库勒式的“错误”,但同样有一些实验证明了凯库勒式的“正确”,只是大部分教材为了简化编写,避免不必要的争论,将这些实验有意无意地忽略了。在这一点上,经典的《基础有机化学》(邢其毅著)教材做得较好,从第一版到第三版,教材中均讲述了苯和邻二甲苯臭氧化实验,而这两个实验正是验证凯库勒式正确性的著名历史性实验。
1904—1905年,就有人进行苯的臭氧化实验,发现反应产物中只有乙二醛,说明臭氧化断键位置确实是在凯库勒式的“双键”位置上;1932年进行了邻二甲苯的臭氧化实验,不仅得到了与凯库勒式预测相同的产物,还进一步支持了凯库勒提出的双键位置来回摆动的设想(这一设想成为共振论的张本)。邻二甲苯臭氧化实验近年来经常作为题目出现在化学竞赛以及高考教辅材料上,可见这一实验的重要程度。
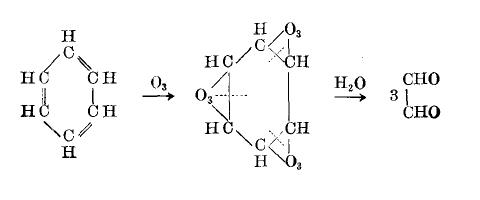
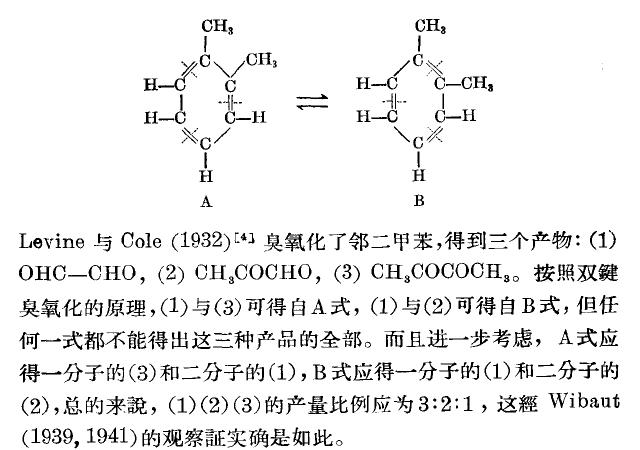
1912年有人以庚二酸作为起始原料,先脱水脱羧生成环己酮,再还原生成环己醇,然后通过逐步生成季铵碱以及霍夫曼消除反应,逐步在环中引入三个双键,最终合成得到的“环己三烯”就是苯,这一实验比三分子乙炔的聚合实验更能说明苯确实是“环己三烯”。
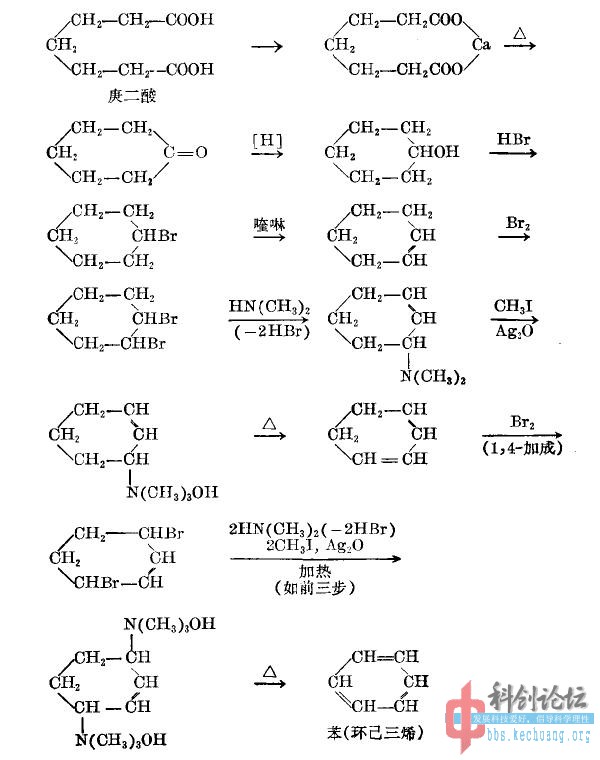
甚至在一些极端条件下,苯环未必不能表现出类似一般共轭双键的性质,用极强的亲双烯体,例如六氟-2-丁炔或者二氰乙炔,可以让均四甲苯中的苯环发生双烯合成反应(D-A反应),苯环完全按照凯库勒式结构发生反应。
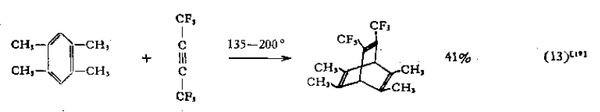
这些实验至少说明,苯环在一定情况下,是以凯库勒式结构参与反应的。
休克尔于1931年提出了休克尔分子轨道法(HMO),并衍生出了著名的休克尔规则,即判断芳香性的4n+2规则,一直在各种有机化学教科书中沿用到今天。但实际上,HMO方法只是一种非常粗糙的半经验方法,休克尔认为σ电子和π电子相互独立,因此计算时只考虑π电子和π键,没有考虑σ电子和σ键,这也就是一般教科书上用MO理论解释苯分子结构时,只考虑π分子轨道的原因。
但HMO方法的出现,有其历史原因,当时没有高性能的计算工具,半经验方法计算量较小,适合当时的实际情况。但在计算机飞速发展的今天,HMO方法的粗糙结果如果一直沿用下去,就有些不合时宜了。1987年Shaik等人用从头计算法得出一个结论:苯分子中的π电子有畸变成为3个定域π键(即“环己三烯”)的趋势。
目前认为,π电子具有两重性,既可能趋向于离域,也可能趋向于定域(双键),而且趋向于定域可能具有更高的稳定性。苯分子中6个C-C键完全等同,或者说正六边形环状结构,不能排除σ键的影响,苯分子中的π电子,是在σ键骨架的强制力作用下,才离域的。苯环的稳定性,应该理解为4n+2 π电子“离域不稳定性”较小,而不是4n+2 π电子“离域稳定性”更大,而π电子是有自发趋向于定域趋势的。1961年,Berry在分析苯分子的振动频率后发现,在单双键交替的“环己三烯”状态,苯分子的停留时间可占整个振动周期的15%——这可不是一个小数字。
邢其毅《基础有机化学》第二版和第三版在讲到苯结构时,也提到了目前的新看法:苯的正六边形结构只决定于σ电子,从本质上看,苯的π体系不倾向于一个离域的“芳香六隅体”,而是倾向于具有三个定域的π键的结构。还提到了两种定域的凯库勒结构是一对“电子互变异构体”的观点。
感兴趣的同学,可以看看中科院虞忠衡的一系列关于“共轭失稳定”的文章,或者看一下百度化学吧中《环己三烯的故事》一文。
理论有机化学和量子化学也是在飞速发展的,不要被几本目前的教科书限制了思维和认识。




200字以内,仅用于支线交流,主线讨论请采用回复功能。