[toc]
看了标题先不要吐槽,因为帖子真是教大家怎么配制饱和溶液的,虽然听起来很低级,但是这一步非常重要的,骗人是小狗
帖子可能有点绕,不过必须要先介绍下过饱和溶液的稳定性,不然后面的内容没办法继续。溶质的溶解度会随温度变化这个应该都知道,这条变化曲线一般就叫作溶解度曲线。不过溶解度曲线并不一条简单上下分明的线,而是在曲线上方有一个小的介稳区,晶体的生长跟这个介稳区有很大关系,可以说晶体就是在介稳区里生长出来的。
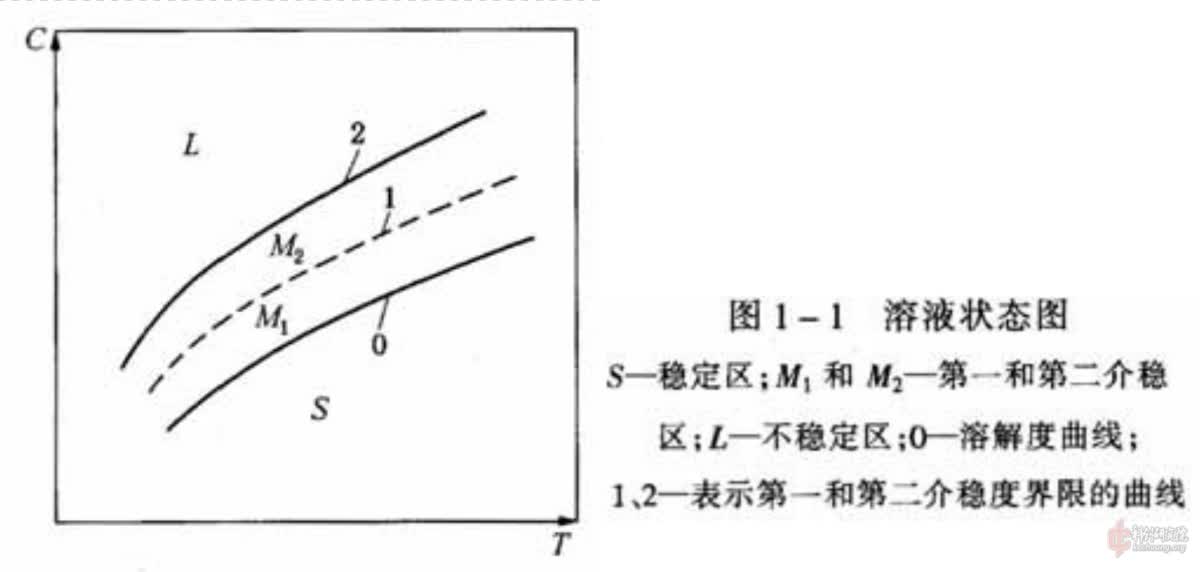
图片截自<化工结晶过程原理及应用> (叶铁林 主编 ISBN:7563916490)
图上 X 轴是溶液温度,Y 轴是溶液浓度,。曲线 0 就是溶解度曲线,0 线下面的 S 区域为稳定的不饱和区。曲线 2 是介稳区上界,再上面的 L 区是溶液不稳定区。曲线 0 和 2 之间的
条件合适的话,溶质会在介稳区里析出生长成晶体。
配制饱和溶液主要目的就是想办法让溶液浓度进入
饱和溶液不好配一个重要原因是我们用肉眼无法判断溶液是否已经饱和,一般只能通过加入溶质然后观察溶质是否还能继续溶解来判断。通过精准称量来配制的话会有另一个难点,手册/文献上查到的溶解度数据一般都是精确测定的数据,测定所使用的试剂和溶剂纯度都比较高,溶液平衡时间也足够长。而我们平时买到的试剂和溶剂纯度一般到不了那个级别,杂质(包括 PH 值)对晶体的溶解度是有比较大影响的。以硫酸铜水溶液为例,假如试剂和水中的杂质使用得硫酸铜溶解度增加了 1%,又因为
我想到的比较可靠的配制方法其实非常简单,就是 —— 往溶液里加过量的溶质然后过滤!含有过量溶质固体的溶液浓度一般落在溶解度曲线 0 上或者稍微线上一点点。过滤时溶液会受到剧烈扰动以及过程中溶剂挥发,得到的滤液会因此会过饱和及自发成核,影响后继使用,生长出我们不想要的晶体来。针对这个问题如何避免,具体操作我有两个比较可行的方案:
先在要盛放滤液的容器里滴几滴溶剂,再进行过滤。这样容器里得到的滤液浓度会在溶解度曲线下面一点点,接着静置溶液待溶剂挥发让溶液浓度进入
滤液获取方法跟前面的方案一样,不同的是如何让溶液恢复饱和状态。这个方案是直接把一颗较大的晶种放进滤液中去,溶解掉一部分的晶种使得溶液达到饱和。要特别注意根据溶解度计算那几滴溶剂会溶解掉多少晶种,千万不要溶剂加多了或者晶种太小了使得晶种完全溶解溶液还未饱和导致晶体生长失败。这个方案的优点是简单方便,只要计算没出错一般不会出大问题,缺点是实操过程中经常出现固定晶种的机构会因为晶体溶解掉一部分而失效。
注意要点:
配溶液一定要搅拌,直接加水猛摇几下然后放置过夜大概率得不到饱和溶液
搅拌时间要足够长,很多晶体溶解速度非常慢,有时要以小时计,比如硫酸铜就是典型
搅拌后静置的时间也要足够长,最好放几小时再过滤
(其实跟网上能搜到的晶体生长 tips 差不多,看过的就再看一遍吧
保证水的纯度。有条件的买娃哈哈瓶装水,一瓶 2 块钱 600mL 那种,随开随用。没有的就买 5L 或 10L 的大桶装那种。实验室的超纯水仪出来的超纯水电阻率一般要到 18MΩ 算合格,电阻率越低说明水纯度越低,家里有电阻率仪的可以自己测一下来判断水的纯度。
试剂要做重结晶,最好可以做两次以上。宏观上,杂质的影响主要有几个:1)改变主结晶物的溶解度 2)影响晶体的生长速度 3)改变晶体的宏观形貌 4)影响溶液的稳定性,可能会使介稳区变宽也可能变榨。这些影响使得晶体生长的可控性降低,实验重现性变差。有些杂质含量百分之几都不会有啥大影响,有些杂质 ppm 级别就会有严重影响,为了你好我好大家好,有条件可以纯化的就纯化一下吧。
只是普通的蒸发法长晶体的话,可以使用一次性的 PET 杯子。淘宝上搜“PET 糕点盒”之类的关键词,选那种器壁光滑的杯子或盖子来用,不需要买培养皿的,那玩意儿太贵了而且一点也不好用。搅拌棒直接买那种一次性塑料滴管代替。玻璃仪器虽然在化学实验里非常好用,但是通常情况下是非常难把玻璃仪器洗干净的,玻璃表面也比较容易被刮花,而且水会浸润玻璃表面,用来长晶体会增加难度。建议全换成一次性用品,用完即弃,一个烧杯 ¥5,可以买 50 个 PET 杯子。
晶体生长尽量让溶液浓度一直保持在
如果你是刚开始学习要长晶体的话,建议先长一些溶解高的带结晶水的晶体。对于我们比较常见的晶体,溶解高或含结晶水的晶体一般会有比较宽的介稳区。强烈不建议长 NaCl KCl 之类的这种不含结晶水的碱金属简单化合物,碱土金属盐也不建议,他们的不少盐溶解度曲线以及他们跟水的相图都比较奇怪,不了解的话容易长出奇怪的东西来。具体的介稳区宽度可以搜索文献查一查数据来参考,关键词用 “metastable zone width” 或用缩写 “MSZW” 也可以(不过要特别注意文献里表示“不饱和度”的时候有很多种表达方式,g/100g 这种溶解度表达比较少用)。文献查不到数据的化合物,等有经验了再长吧。
尽量保持溶液温度稳定。这个其实非常非常重要。但因为业余条件不太好操作,就不具体写了,大家知道这个有影响就行了,实际操作随缘吧。
附一些

这个表格是从这本书上截的,书是网上随便搜的,我核对了几个表格里的数据,跟别的文献能对得上,因为这个表格列的化合物种类比较多所以就截过来了。书名似乎叫 <CHEMICAL ENGINEERING>,ISBN 是多少没有去查。表格上
Crystallization of Copper Sulphate (M Giulietti 1995 DOI:https://doi.org/10.1002/crat.2170300206)
Metastable zone-width of some aqueous solutions (Jaroslav Nývlt 1970 DOI: https://doi.org/10.1016/0022-0248(70)90034-5)
Crystallisation of copper sulphate pentahydrate from aqueous solution in absence and presence of sodium chloride (F.J. Justel 2019 DOI:https://doi.org/10.1016/j.jcrysgro.2019.125204)
过年前原本想写点杂质对晶体生长的影响相关内容的,为此啃了好长时间的生长动力学,后来发现这个太复杂而且涉及到的概念和背景知识很多,年前俩月工作太忙就先搁置了。年后过来改成先写写重结晶过程,因为重结晶跟杂质对晶体生长的影响是相关的,涉及的东西却少了很多,构思到一半发现要写完依然还是得介绍很多概念,估计要写很久。。。只好再再缩小范围,先写一下怎么配制饱和溶液吧,这个涉及的东西比较少,一个帖子应该就能写得完,而且实验操作简单,可以不用特地做个实验啥的来支撑帖子内容。
ps: 帖子不是一个 step-by-step 教程,所以如果你问关于操作上的一些细节问题的话我可能也不一定懂。比如要加热到多少度,怎么过滤,用什么滤纸,如何保温如何防尘什么的,这些不知道的我可能会假装没看到:)
帖子的理论内容大部分都来自于 <化工结晶过程原理及应用> (叶铁林 主编 ISBN:7563916490) 这本书的第二章第一二节(书里还有不少大家喜欢的化肥生产相关内容,附录里有很多化合物的溶解度密度表格,对想用复分解法做一些奇怪东西的同学很有用),如果帖子看得比较迷糊的话可以自己读一下这部分的内容,一些名词概念看不懂的先维基上看一下,书里涉及到的概念会更多。实操部分则是我脑补的,我自己没实践过,不保证一定能成功。